Миелобласт
Содержание
- 1 Морфология клеток миелоцитарного (гранулоцитарного) ростка
- 1.1 Микрофотографии миелобластов:
- 1.2 Микрофотографии промиелоцитов:
- 1.3 Микрофотографии нейтрофильных миелоцитов:
- 1.4 Микрофотографии эозинофильных миелоцитов:
- 1.5 Микрофотографии палочкоядерных эозинофилов:
- 1.6 Микрофотографии зрелых (сегментоядерных) нейтрофилов:
- 1.7 Микрофотографии зрелых эозинофилов:
- 1.8 Микрофотографии зрелых базофилов:
- 2 Миелобластные лейкозы: причины развития и методы терапии
- 3 Острый и хронический миелобластный лейкоз
- 4 Хронический и острый миелобластный лейкоз крови
Морфология клеток миелоцитарного (гранулоцитарного) ростка
Гранулоциты — клетки, в цитоплазме которых обнаруживается зернистость, специфическая для определенного вида клеток. Различают нейтрофильную, эозинофильную и базофильную зернистость.
См. также: Подсчет миелокариоцитов
Нейтрофильная зернистость розовато-фиолетовой окраски, чаще пылевидная, обильная, не всегда равномерно заполняет цитоплазму.
Эозинофильная зернистость однородна по цвету, форме и величине, крупная, занимает всю цитоплазму. В зрелых клетках имеет кирпично-розовый цвет (кетовая икра), в молодых эозинофильных лейкоцитах — коричневый и буро-синий оттенок.
Базофильная зернистость чаще фиолетового, реже черного цвета, неоднородна по величине и форме, обычно необильна, располагается на ядре и в цитоплазме.
Миелобласт — родоначальная клетка гранулоцитарного ряда. Размер клетки — 10 — 20 мкм. Форма чаще круглая, иногда овальная. Ядро занимает большую часть клетки, круглое или овальное, окрашивается в красно-фиолетовый цвет.
Хроматин — мелкосетчатый. Ядерная мембрана очень тонкая. В ядре можно обнаружить от 2 до 7 ядрышек, окрашивающихся в светло-синий, а иногда в красновато-фиолетовый цвет.
Цитоплазма базофильная, содержит небольшое количество неспецифических азурофильных гранул.
Микрофотографии миелобластов:
Myeloblast, late neutrophil, normal marrow
Myeloblast, neutrophilic metamyelocyte, normal marrow
Myeloblast, late NRBC, normal marrow
Промиелоцит образуется в процесе деления миелобласта, далее из него образуются более зрелые зернистые лейкоциты. Величина клетки колеблется от 12 до 24 мкм. Ядро занимает большую часть клетки, красно-фиолетовое. Форма ядра круглая, овальная или с небольшим вдавлением, располагается чаще эксцентрично.
Структура ядра сетчатая, местами более грубая. Ядерная мембрана тонкая. В ядре могут быть видны ядрышки, которые не всегда хорошо выражены. Цитоплазма промиелоцитов чаще имеет значительные размеры, иногда образует небольшой ободок.
У более молодых клеток окрашивается в разные оттенки синего цвета, по мере созревания клеток приобретает розовато-голубой цвет. Промиелоцит — первая клетка гранулоцитарного ряда, в которой появляется специфическая зернистость.
В зависимости от типа специфической зернистости промиелоцит относят к нейтрофильному, эозинофильному или базофильному ряду. Можно видеть и довольно крупную недифференцированную зернистость (типа азурофильной), окрашивающуюся преимущественно в красно-фиолетовый цвет.
Эозинофильные гранулы на разных этапах развития содержат большое количество кислой базофильной субстанции, воспринимающей щелочные (синие) краски, поэтому большинство гранул окрашивается в грязновато-синий цвет. Такие клетки можно ошибочно принять за базофильные.
Во избежание ошибки следует учитывать не только окраску, но и размеры, форму гранул: в клетках эозинофильного ряда они правильной округлой формы и одинакового размера, а в клетках базофильного ряда величина их колеблется от мелких точечных до крупных хлопьевидных образований неправильной формы.
Промиелоциты нередко трудно отдифференцировать от молодых миелоцитов. Основное отличие — расположение зернистости в клетке: у промиелоцита она располагается и в цитоплазме, и на ядре, а у миелоцита — только в цитоплазме.
Микрофотографии промиелоцитов:
Progranulocyte, band neutrophils
Progranulocyte, band neutrophils, normal marrow
Progranulocyte, myelocyte, normal marrow
Размер миелоцита — 8 — 18 мкм. В миелоцитах различают две генерации — крупные незрелые материнские миелоциты и меньших размеров зрелые дочерние миелоциты. Дочерние миелоциты образуются из материнских в результате пролиферации и дифференциации.
Ядра миелоцитов сочные , с характерным чередованием более светлых и более темных участков хроматина. Рисунок хроматина в ядре зависит от степени зрелости клеток: более мелкий, сглаженный, рыхлый — у незрелых миелоцитов и более крупный, грубый и густой — у зрелых.
Материнскому миелоциту свойственно ядро рыхлой структуры, как бы набухшее, а дочернему — овальное, бобовидное или бухтообразное, глыбчатое. Ядрышки в ядре миелоцита, как правило, отсутствуют.
Цитоплазма нейтрофильного миелоцита окрашивается в светлый сине- или фиолетово-коричневый тон у материнских форм и розоватый — у дочерних. В центре клетки, вблизи ядра, в области расположения комплекса Гольджи окраска цитоплазмы менее интенсивна.
По наличию этого просветления в цитоплазме миелоциты можно легко дифференцировать даже в тех случаях, когда зернистость плохо окрашена или совсем не окрашена (при лейкозах).
Зернистость мелкая, такого же типа, как и у зрелых нейтрофильных гранулоцитов, но среди мелких гранул всегда располагаются и более крупные.
Цитоплазма эозинофильного миелоцита окрашивается в голубой цвет, густо «нафарширована» эозинофильной (ярко-оранжевой) зернистостью, среди которой могут встречаться гранулы синего или фиолетово-красного цвета (более молодая эозинофильная зернистость).
Цитоплазма базофильного миелоцита также окрашивается в голубой цвет. Зернистость отличается колебаниями в оттенках окраски отдельных гранул (темно-синяя, синяя, фиолетово-красная), форме и количестве гранул.
В нормальных условиях только дочерние миелоциты через метамиелоциты переходят в полиморфные лейкоциты.
Материнские миелоциты, не давшие дочерних генераций, могут в дальнейшем развиваться в зрелые полиморфные лейкоциты только в патологических условиях. Такие лейкоциты имеют большую величину и большее количество сегментов в ядре.
Кроме этого при патологических процессах, особенно при лейкозах, в миелоцитах отмечается несоответствие в развитии ядра и цитоплазмы, а также зернистости клеток.
Микрофотографии нейтрофильных миелоцитов:
Late neutrophilic myelocyte, normal marrow
Neutrophilic myelocyte, normal marrow
Myelocytes, abnormal platelets, AML blood
Myelocyte, disrupted band neutrophil
Микрофотографии эозинофильных миелоцитов:
Eosinophilic myelocyte, Normal marrow
Eosinophilic myelocyte, neutrophilic myelocyte
Eosinophilic myelocyte, eosinophilic metamyelocyte, mitosis
Eosinophilic myelocyte, neutrophilic myelocytes
Размер палочкоядерных гранулоцитов — 9 — 12 мкм. Ядерно-цитоплазматическое отношение сдвинуто в пользу цитоплазмы. Ядро имеет вид палочки (часто изогнутой), иногда с сужениями, сохраняющими двухконтурность. Хроматин грубой структуры.
У нейтрофильного палочкоядерного гранулоцита цвет цитоплазмы розоватый с фиолетовым оттенком; зернистость большей частью обильная, но не всегда равномерно заполняет цитоплазму.
У эозинофильного палочкоядерного гранулоцита цитоплазма неясного голубого цвета, мало заметного из-за обильной эозинофильной зернистости.
Базофильные палочкоядерные гранулоциты практически не встречаются.
Микрофотографии палочкоядерных эозинофилов:
Band eosinophil, mature neutrophil, Normal blood
По размеру и ядерно-цитоплазматическому соотношению cегментоядерные гранулоциты аналогичны палочкоядерным гранулоцитам. Ядро полиморфное, разделено на сегменты, соединенные тонкими одноконтурными перемычками, окрашивается в темно-фиолетовый цвет.
Ядра нейтрофильных сегментоядерных гранулоцитов имеют в норме 2 — 5 сегментов, цитоплазма розовая или розово-фиолетовая, содержит нейтрофильную зернистость.
Ядра эозинофильных сегментоядерных гранулоцитов имеют обычно 2 сегмента, реже 3 или 4. Цитоплазма заполнена эозинофильной зернистостью.
Базофильный сегментоядерный гранулоцит имеет трехсегментированное или лопастное ядро. Цитоплазма бледно-розового или фиолетового цвета. Крупная темно-фиолетовая зернистость располагается и на ядре, и в цитоплазме.
Микрофотографии зрелых (сегментоядерных) нейтрофилов:
Mature Neutrophils, Platelet Satellitism
Young megakaryocyte, neutrophilic myelocytes, normal marrow
Segmented neutrophils, band neutrophils, normal blood
Микрофотографии зрелых эозинофилов:
Eosinophil, Normal blood
Eosinophil, Normal blood
Микрофотографии зрелых базофилов:
Basophils, mature neutrophils, CML blood
Basophil
Basophil
Все вышеописаные клетки в соответствующих количествах встречаются в нормальном костном мозге, в периферической крови взрослого человека в норме встречаются только зрелые клетки — палочкоядерные и сегментоядерные гранулоциты.
В ряде случаев, при наследственных или приобретенных патологических состояниях, в гранулоцитах наблюдаются определенные морфологические нарушения (изменения), которые можно разделить на две группы: дегенеративные изменения и конституциональные аномалии.
- Л. В. Козловская, А. Ю. Николаев. Учебное пособие по клиническим лабораторным методам исследования. Москва, Медицина, 1985 г.
- Руководство к практическим занятиям по клинической лабораторной диагностике. Под ред. проф. М. А. Базарновой, проф. В. Т. Морозовой. Киев, «Вища школа», 1988 г.
- Руководство по клинической лабораторной диагностике. (Части 1 — 2) Под ред. проф. М. А. Базарновой, академика АМН СССР А. И. Воробьева. Киев, «Вища школа», 1991 г.
Основным местом образования лимфоцитов служит кроветворная ткань селезенки и лимфатических узлов. В костном мозге и периферической крови в норме встречаются только зрелые лимфоциты. При патологии в костном мозге и периферической крови могут появляться незрелые и атипические формы клеток лимфоидного ростка.
Раздел: Гемоцитология
Читать
Монобласт — родоначальная клетка моноцитарного ряда. Размер 12 — 20 мкм. Ядро большое, чаще круглое, нежносетчатое, светло-фиолетового цвета, содержит 2 — 3 ядрышка. Цитоплазма монобласта сравнительно небольшая, без зернистости, окрашена в голубоватые тона.
Раздел: Гемоцитология
Читать
Ретикулярные клетки довольно большого размера (18-30 мкм). Ядро круглое или овальное, структура ядра ажурная, иногда неравномерно-нитчатая и напоминает ядро моноцита, может содержать 1-2 ядрышка.
Цитоплазма обильная, чаще всего с нерезко очерченными границами, нередко отростчатая, окрашивается в светло-голубой или серовато-голубой цвет, иногда содержит пылевидную азурофильную зернистость.
В норме эти клетки в пунктате костного мозга содержатся в небольшом количестве.
Раздел: Гемоцитология
Читать
К морфологически идентифицируемым клеткам эритроцитарного ростка относятся эритробласт, пронормоцит, нормобласты (базофильные, полихроматофильные и оксифильные), ретикулоциты и эритроциты.
Раздел: Гемоцитология
Читать
Патологические формы эритрокариоцитов (эритробластов и нормобластов) наблюдаются при некоторых патологических состояниях (острый сепсис, апластические анемии, острый лейкоз, тяжелые инфекционные заболевания, после облучения и др.). Изменяется морфология ядра и цитоплазмы клеток различных стадий созревания.
Раздел: Гемоцитология
Читать
Источник: http://www.clinlab.info/Hemocytology/Cell-morphology-of-myelocytic-granulocytic-series-1
Миелобластные лейкозы: причины развития и методы терапии
Миелобласты – это первые клетки нейтрофильных, базофильных и эозинофильных ростков. Причем, у каждого из них на начальном этапе созревания нет морфологических отличий. Миелобласт напоминает лимфоцит с несколькими ядрышками.
В здоровом костном мозге человека базофильные клетки встречаются при хроническом течении миелолейкоза, а эозинофильные – когда отмечаются эозинофилии.
Миелобластные лейкозы развиваются в результате нарушений созревания элементов в процессе кроветворения.
Следует отметить, что созревающие клетки включают:
- Промиелоциты;
- Нетрофильные миелоциты;
- Эозинофильные;
- Базофильные.
Миелоциты способны к делению, но при переходе на следующий этап созревания образуются метамиелоциты. Эти клетки считаются «юными».
Зрелые элементы делятся на палочкоядерные и полиморфноядерные. Весь период созревания длиться 2 недели. После этого клетки миелоидного ростка приобретают способность к фагоцитозу и начинают двигаться к сосудистому руслу. Нейтрофилы циркулируют по крови до 10 часов, а затем проникают в ткани организма.
Острый миелобластный лейкоз относится к опухолевым новообразованиям. Оно развивается в результате перерождения миелоидного ростка. Кровяные клетки замещают полноценные элементы лишь на часть или устраняют их из кровеносного русла совсем. Но, поскольку новообразования не могут выполнять функции нормальных миелоцитов, то у человека развивается рак крови.
Миелобластный лейкоз крови рассказывает о том, что в кровяном русле больного распространяется огромное количество лейкоцитов. Источником образования белых телец является костный мозг. Он в определенный момент начинает продуцировать нездоровые бласты.
Несмотря на то, что лейкоциты – это защитные клетки иммунитета, отвечающие за здоровье человека, в данном случае неполноценные или дефектные элементы только переполняют кровь, проникая во все ткани и органы.
Так, они нарушают функцию иммунной и других систем организма.
Миелобластный лейкоз крови говорит о том, какие элементы лейкоцитарной популяции преобразовались в предшественников опухолевого образования. Как уже упоминалось выше, лейкоциты бывают нейтрофильными и лимфоцитарными.
Поскольку миелоидный росток производит не только нейтрофилы, но и тромбоциты, эритроциты, при лейкозной опухоли обязательно развивается анемия. У больного отмечается падение гемоглобина и резкое сокращение объема эритроцитов в крови.
Также наблюдается тромбоцитопения, что ведет к появлению кровотечений.
Если развивается острый миелобластный лейкоз, то заболевание прогрессирует очень быстро. Прогрессивное производство незрелых лейкоцитов в короткие сроки замещает нормальные элементы крови и у пациента снижается вероятность выздоровления.
Хронический миелобластный лейкоз развивается длительное время и в начальных этапах не проявляется никакими симптомами. Интересно, что при ХМЛ у людей практически всегда обнаруживают филадельфийскую хромосому.
Поэтому риск заболеть данной формой опухоли увеличивается у пациентов с генетическими аномалиями.
Острый миелобластный лейкоз: причины возникновения и основные симптомы
Нельзя назвать конкретный негативный фактор, который способен изменить функциональность костного мозга. ОМЛ относят к многопричинным болезням, возникновение, которого сложно уточнить. Кроме того, даже, когда установить первопричину опухолевого процесса удалось бы, терапия источника деформации миелоцитов не становится вероятной.
Острый миелобластный лейкоз сможет развиться из-за активации следующих факторов:
- Ионизирующее излучение – действие радиации (атомные взрывы);
- Химический канцерогенез – воздействие пестицидов, гербицидов, других химических токсинов;
- Биологические онкогенные вирусы, трансформирующие здоровые элементы в опухолевое поражение миелоидного ростка.
Несмотря на точную причину развития острого миелобластного лейкоза, результатом ее действия становится повреждение ДНК кровяных телец. В этом случае ген, отвечающий за нормальную гибель клеток, почему-то перестает работать. Таким образом, опухолевые новообразования приобретают бессмертие, несмотря на полную дисфункцию и искажение клеточной структуры.
К симптомам ОМЛ относят различные проявления организма. Клиническое течение онкозаболевания зависит от того, какие системы были поражены – ЦНС, ЖКТ, печень, кости, лимфоузлы и т.д.
Симптомы острого миелобластного лейкоза:
- Ежедневное недомогание, усталость, ослабленность;
- Повышенное потоотделение без особых причин;
- Бледность кожи;
- Отечность ног, рук;
- Появление одутловатых отеков на лице и шее;
- Высокая температура;
- Увеличение лимфоузлов;
- Болезненность в мышечных, костных тканях;
- Учащение сердцебиения, одышка;
- Поносы, рвота, тошнота;
- Увеличение печени, селезенки;
- Кровотечения, ломкость капилляров;
- Частые респираторные болезни, грибковые инфекции;
- Неврологические расстройства;
- Головные боли.
Клиническая картина с широким спектром симптомов зависит от того, что кровь распространяется по всему организму, поэтому при переизбытке опухолевых лейкоцитов в одном из органов начинают проявляться характерные признаки болезни. Особенно часто отмечается поражение тех тканей, которые отличаются хорошим кровоснабжением. Важно отметить, что симптомы не проявляются в один момент, а постепенно присоединяются друг к другу.
Хронический миелобластный лейкоз имеет похожие признаки. Но есть одно отличие – в некоторых случаях болезнь провоцирует инсульт. Это объясняется тем, что на каком-то этапе организм начинает вырабатывать большое количество тромбоцитов. Так, кровь густеет и повышается риск образования тромбов.
Лечение миелобластного лейкоза: основные методы
Поскольку чаще всего онкологической опухолью болеют дети, то терапия ОМЛ рассчитана на оздоровление юных организмов. В первую очередь, пациенты с миелобластным лейкозом обязательно направляются на химиотерапию. Курс лечения интенсивный и продолжительный, ведь от него зависит прогноз здоровья больного человека.
В некоторых случаях дополнительно применяют облучение головы и высокодозированную химиотерапию. После этих процедур трансплантируют стволовые клетки. Точный метод лечения и его продолжительность устанавливают после определения индивидуальных особенностей больного. Также учитывают шансы на излечение у конкретного пациента.
Лечение миелобластного лейкоза проводится с целью уничтожить все раковые клетки, после чего костный мозг сможет начать выработку здоровых кровяных элементов. Чтобы во время проведения всех процедур предупредить развитие осложнений, дополнительно назначают сопроводительную терапию. Это очень важный этап комплексного лечения пациентов с ОМЛ, от которого зависит прогноз выздоровления.
Терапия острого миелобластного лейкоза проводится в несколько ступеней. Каждый этап лечения отличается продолжительностью, группами использующихся препаратов, поставленными целями.
Самая первая интенсивная химиотерапия, которая позволяет за короткий период уничтожить максимальное количество лейкозных клеток. После этого у пациента наступает ремиссия.
Дальше проводится еще один курс интенсивной химиотерапии. Но теперь назначают дополнительные медикаменты и повышают дозировку препаратов. Если после индукции какие-то опухолевые клетки остаются живыми, то консолидация дает возможность уничтожить их полностью. Также на данном этапе снижается риск возврата заболевания.
Чтобы защитить головной и спинной мозг от проникновения опухолевых лейкоцитов, пациентам обязательно делают превентивное введение медикаментов в спинномозговой канал. Эта процедура не дает возможности распространяться раковым клеткам по ЦНС. Если же миелобласты уже проникли в центральную НС, тогда пациентам проводят облучение головного мозга.
Чтобы предотвратить повторное накопление опухолевых лейкоцитов в крови больного, ему еще на протяжении года проводят поддерживающее лечение. На данном этапе амбулаторно вводят небольшие дозы химиопрепаратов. Таким образом, удается уничтожить все раковые клетки, которые остались живыми после интенсивной терапии.
Если у пациентов в крови накопилось слишком большое количество опухолевых лейкоцитов, то им до начала основной терапии проводят предварительное введение медикаментов. Тем, у кого есть синдром Дауна, назначают совсем другой вид лечения. Это же касается больных с промиелоцитарным лейкозом.
Когда детям не трансплантируют стволовые клетки, то весь срок терапии растягивается на полтора года. Но это относится к тем случаям, когда после химиотерапии не случалось рецидива онкозаболевания.
Прогноз лечения миелобластных лейкозов в настоящее время улучшился. Если раньше пациенты с острым МЛ умирали уже на втором этапе развития опухоли, то сейчас применение химиотерапии сильно изменили ситуацию.
Статистические данные показывают, что половина всех больных полностью излечиваются от онкологии и у них не случается рецидивов на протяжении всей жизни.
В других же случаях удается значительно продлить периоды ремиссии.
Миелобластные лейкозы, особенно острой формы, тяжелые онкоболезни, но при правильном лечении и своевременном использовании химиотерапии есть высокая вероятность излечиться от этого коварного врага. Главное вовремя обращать внимание на негативные симптомы.
Источник: https://diagnos-med.ru/mieloblastnye-lejkozy-prichiny-razvitiya-i-metody-terapii/
Острый и хронический миелобластный лейкоз
Миелобластный лейкоз — это опухолеподобное заболевание крови, вызванное чрезмерным развитием промежуточных клеток лейкоцитарного ряда (гранулоцитов). Болезнь возникает в острой или хронической форме. Поражает людей разного возраста и пола. Особенностью миелобластных лейкозов, как и других, является отсутствие перехода острой формы в хроническую.
Это разные заболевания, со своей клиникой, стадиями течения, прогнозом. Название связано с преимущественной ролью в патогенезе вида промежуточных незрелых лейкоцитов.
У детей миелобластный лейкоз (острый) составляет 15% онкопатологии. Обнаруживают ежегодно менее 1-го больного в расчете на 100 тысяч детей. Значительный рост заболеваемости происходит в возрасте 40 – 45 лет и у пожилых.
Зачем нужны миелобласты?
Миелобластами называются клетки-прародители гранулоцитов, к которым относятся нейтрофилы, эозинофилы, базофилы (клетки миелоидного ряда). Они вместе составляют свыше 80% всех лейкоцитов.
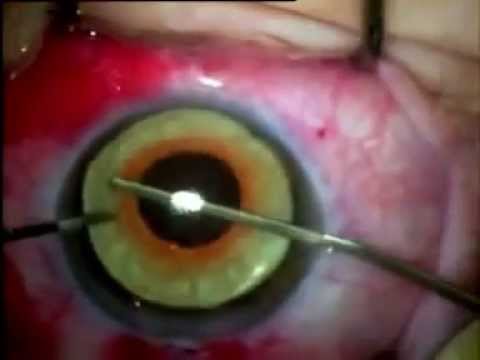
Так выглядит миелобласт под микроскопом
Главное отличие миелобластов от других клеток крови — крупный размер и большое ядро. При анализе периферической крови иногда попадают в поле зрения лаборанта, потому что небольшая часть свободно циркулирует по кровяному руслу.
Другая, основная часть, находится в костном мозге, селезенке, лимфоузлах и обеспечивает с помощью своего деления производство следующих клеток — промиелоцитов, которые дозревают до нормальных гранулоцитов.
Баланс между «прародителями» и рабочими клетками обеспечивается нуждами организма. Только вполне зрелые клетки могут выполнять защитную функцию и обеспечивать достаточный иммунитет.
Сбой процесса дозревания миелоцитарных клеток приводит к излишнему накоплению их в составе крови. При этом резко падает количество «трудоспособных» элементов, нарушаются многие функции организма.
Причины
Причиной, вызывающей нарушенное кроветворение, в настоящее время считается изменение состава и структуры хромосом человека. Оно может возникнуть у детей и у взрослых под воздействием мутагенных факторов:
- излучение радиации;
- распространение химических агентов, особенно бензола, в лакокрасочной промышленности, при выделке кож;
- лечение препаратами цитостатического действия и иммунодепрессантами;
- наследственная неустойчивость миелоцитов.
Клинические проявления, симптомы и течение зависят от формы заболевания.
Клиника острого миелоцитарного лейкоза
Наиболее частая форма лейкоза у взрослых. Опухолевые миелобластные клетки разрастаются и наполняют костный мозг, селезенку, лимфатические узлы, печень, слизистую оболочку желудка и кишечника.
В 30% случаев они расположены в легочной ткани, в 25% — в мозговых оболочках. Одновременно блокируется нормальное развитие тромбоцитов и эритроцитов.
По преобладанию нарушений состава крови выделяют семь типов острого миелобластного лейкоза.
Клинические проявления обусловлены подавлением конкретного ростка крови:
- при снижении количества эритроцитов основными являются симптомы малокровия (анемии) — бледность кожи, повышенная утомляемость, головные боли и головокружение, одышка при нагрузке;
- если снижены тромбоциты, возникают кровотечения различной тяжести (носовые, маточные, желудочные), на теле появляется множество кровоподтеков;
- лейкопения приводит к частым инфекционным заболеваниям с затяжным течением, осложнениями, артритам.
Клиника хронического миелобластного лейкоза
Хронический миелобластный лейкоз, в отличие от острого, вызван разрастанием более молодых и зрелых клеток, а не бластов. Но они также подавляют развитие эритроцитарного и тромбоцитарного ростков. Заболевание может длиться много лет. В течении болезни различают три стадии.
Начальная не имеет практических симптомов, выявляется случайно. Ретроспективно установлен такой лабораторный симптом, как лейкоцитоз неясного происхождения. У некоторых пациентов имеется небольшое увеличение селезенки, которое вызывает редкие тупые боли в левом подреберье, чувство тяжести, переедания. Количество тромбоцитов в крови даже увеличивается.
Развернутая — начинается лейкемическая инфильтрация, появляются клинические симптомы:
- повышенная потливость;
- утомляемость и слабость;
- постоянная невысокая температура тела;
- похудение;
- боли и тяжесть после ходьбы в левом подреберье, отдающие в левое плечо, усиливаются при дыхании;
- тошнота, потеря аппетита;
- желтушность кожи и слизистых;
- боли в области сердца, аритмия.
Желтушность склер и кожи
Симптомы связаны с поражением печени, селезенки, интоксикацией билирубином, нарастанием анемии. Длительность стадии без лечения — от полутора до 2,5 лет, при лечении — 5 и более.
Терминальная — резко ухудшаются все проявления, повышается температура до значительных цифр, появляются сильные боли в костях, геморрагическое осложнение (частые носовые кровотечения).
Лейкемические инфильтраты вызывают локальные изменения по месту расположения:
- подкожные лейкемиды;
- радикулитные боли (по ходу нервных корешков);
- менингеальные симптомы (в оболочках мозга);
- на слизистых оболочках (шубы, кишечник) возникает сначала воспаление, затем изъязвление.
Больные подвергаются тяжелым инфекционным осложнениям, служащим причиной смерти. Длительность стадии — от полугода до года.
В терминальной стадии возможно появления бластных кризов, когда в кровь выбрасывается множество миелоцитов. При таком течении проводится дифференциальная диагностика с острой формой болезни.
Также прочитать:
Острый лимфобластный лейкоз
Режим и питание больного
Пациентам во время амбулаторного лечения рекомендуется сокращение физических нагрузок, отказ от курения и алкоголя. Для питания необходимы калорийные мясные продукты, свежие овощи и фрукты. Не рекомендуются консервы, продукты с пищевыми заменителями.
При наличии инфильтратов в ротовой полости и по ходу кишечника рекомендуется перетертая щадящая пища.
Необходимы прогулки на свежем воздухе, ношение защитной маски.
Лечение острого миелолейкоза
При выявлении острого лимфобластного лейкоза применяют лечение химиотерапевтическими средствами, действующими на миелоциты (Цитарабин, Даунорубицин, Доксорубицин). Их отрицательный эффект — выраженные побочные реакции в виде тошноты, рвоты, нарастания слабости, повышения чувствительности к любым инфекциям.
Больных в стационарах содержат в боксированных условиях, персонал и родственники постоянно носят марлевые маски для предупреждения передачи инфекции при разговоре.
У большей части больных через несколько недель наступает улучшение. В анализах крови не обнаруживают миелоцитов.
Схема лечения изменяется лечащим гематологом. Необходимо продлить ремиссию. Для этого используют трансплантацию костного мозга. Миелобластный лейкоз лечится либо своим, отобранным перед химиотерапией и замороженным костным мозговым веществом, либо подбирается донор среди кровных родственников.
После каждой трансплантации гематологи ожидают реакцию отторжения чужеродной ткани. Это может сильно осложнить течение болезни. В гематологических клиниках Европы начато использование стволовых клеток.
Лечение хронического миелолейкоза
При хронической форме миелолейкоза лечение начинается после обследования и подтверждения диагноза. Основные препараты для химиотерапии: Миелосан, Миелобромол, Гексофосфамид, Меркаптопурин. С их помощью стараются избежать бластного криза.
Использование дозированной лучевой терапии позволяет затормозить выработку бластных клеток. Противопоказано облучение при значительной тромбоцитопении, выраженном малокровии.
Пациенты подолгу лечатся в стационаре
При нарушении эритроцитарного кроветворения назначают Гемостимулин, курсы витаминов, Ферроплекс, переливание крови.
В терминальной стадии добавляются высокие дозы Преднизолона, симптоматические препараты.
Прогноз
Прогноз заболевания при острой форме у взрослых относительно благополучен: полной ремиссии удается добиться у ¼ пациентов, неполной — до 80%.
У детей, хотя появление острого миелобластного лейкоза бывает редко, болезнь отличается выраженной интоксикацией, резким увеличением печени и селезенки, ремиссии достичь трудно. Выживаемость составляет 17 месяцев после диагностики заболевания.
При хроническом миелобластном лейкозе средняя выживаемость пациентов — 4,5 года, при хорошей реакции на лечение — до 15 лет.
Обмен мнениями позволяет выработать единые стандарты лечения
Проблемы «у нас» и «у них»
Лечением и разработкой оптимальных комбинаций цитостатической и лучевой терапии занимаются ведущие ученые мира. Ежегодно появляются новые препараты, методики лечения.
В июне 2015 года в Москве прошла международная конференция специалистов по онкогематологии. В докладах европейских и российских ученых прозвучали общие мнения:
- не может существовать профилактика лейкозов, поскольку возникновение заболевания носит характер случайности, это похоже на профилактику молнии;
- рост заболеваемости в России связан с улучшением диагностики и ранним выявлением, а в Европе — со старением населения;
- до 40% лиц с миелобластным лейкозом могут иметь длительные ремиссии;
- показатели эффективности лечения в России и в Европе одинаковые;
- задерживается распространение трансплантации костного мозга из-за отсутствия в РФ финансового обеспечения операции, а в европейских клиниках — это дело государства, доноры денег не получают;
- существенная проблема лечения — дороговизна лекарств.
Источник: http://serdec.ru/bolezni/ostryy-hronicheskiy-mieloblastnyy-leykoz
Хронический и острый миелобластный лейкоз крови
В международной классификации болезней, миелобластный лейкоз – это группа болезней под общим названием «Миелоидный лейкоз (миелолейкоз)» C92, в которую включены 8 типов заболеваний, относящихся к злокачественным новообразованиям кроветворной ткани. Самыми распространённые среди них считаются острый (С92.0) и хронический (С92.1) миелоидные лейкозы.
В целом, такие лейкозы характерны видоизменением миелобластов – клеток, предшествующих лейкоцитам.
Благодаря нарушениям в разных хромосомах, которые к тому же возникают на разных стадиях клеточного формирования, бластные клетки не только останавливаются в развитии, но и прекращают узконаправленную специализацию до зрелых форм лейкоцитов: нормобластов, лимфоцитов, моноцитов, эозинофилов и базофилов. Комбинация таких генных изменений с мутацией, вызывающей утрату контроля клеточного размножения, собственно и вызывают лейкоз.
Типы и разновидности миелобластного лейкоза
В большинстве случаев, когда употребляются медицинские термины «острый» и «хронический», то речь идёт о стадии развития или форме одного и того же заболевания. Но в данном случае, острый и хронический миелобластные лейкозы – это 2 разных типа болезни крови, которые отличаются причинами, условиями и механизмом зарождения, поздними симптомами, течением, терапией и прогнозом выживаемости.
Острый тип
Острый миелобластный лейкоз (ОМЛ) – это злокачественное новообразование миелоидного ростка крови, для которого характерно неконтролируемое и очень быстрое деление изменённых форм лейкоцитов.
Накапливаясь в красном костном мозге, они угнетают его работу по воспроизводству других форменных элементов крови — эритроцитов и тромбоцитов. Тем самым это заболевание представляет реальную угрозу жизни – без советующей терапии и в зависимости от разновидности, больной проживёт всего несколько месяцев или недель.
Слева — кровь в нормальном состоянии, справа — при лейкозе
Эта болезнь настолько разнообразна, что существует несколько её классификаций, основная задача которых заключается в оказании помощи онкологам и гематологам – чёткая и углублённая дифференциация помогает принять правильную стратегию терапии.
По классификация Всемирной системы острый миелобластный лейкоз разделён на подгруппы по причинам возникновения:
- генетические видоизменения – описано 9 мутаций генных комбинаций;
- с предшествующей миелодисплазией – 3 подтипа с 17-ю комбинациями генов;
- как следствие предыдущей лучевой или химиотерапии;
- миелоидная саркома;
- сопутствующая болезни Дауна;
- вызванная бластным плазмацитоидным дендритноклеточным новообразованием;
- другие причины, в том числе 10 конкретно описанных разновидностей.
Версия франко-британско-американской классификации (ФАБ)
| ПОДВИД | УТОЧНЁННОЕ НАЗВАНИЕ ОМЛ | ГЕННЫЕ ИЗМЕНЕНИЯ В КЛЕТКАХ |
| М0 | с min дифференциацией | в бластных лейкоцитах отсутствуют гранулы |
| М1 | без созревания | преобладают юные миелоидные клетки |
| М2 | с созреванием | мутация 8 и 21 хромосом |
| М3 | промиелоцитарный | преобладание данных незрелых гранулоцитов |
| М4 | миеломоноцитарный | довлеют миелобласты, монобласты, промоноциты |
| М4ео | с эозинофилией косного мозга | инверсия 16 хромосомы (возможно 8-12 и 11-19) |
| М5 | монобластный и моноцитарный | баланс между монобластами и промоноцитами |
| М6 | 5 типов эритроидного лейкоза | мутация предшественников эритробластов |
| М7 | мегакариобластный | преобладают юные изменённые тромбоциты |
| М8 | базофильный | мутация разных форм незрелых базофилов |
Острый миелобластный лейкоз, в самой упрощённой версии, включает в себя 5 подтипов:
- Миелоидный;
- Миелоидномоноцитарный;
- Моноцитарный;
- Эритроидный;
- Мегакариоцитарный.
В отличии от острого лимфобластного лейкоза, поражающего в основном детей, острый миелобластный лейкоз может возникнуть в любом возрасте. При этом наблюдается закономерность – чем старше возрастная группа, тем больше количество заболевших.
И хотя доля острых миелоидных лейкозов со смертельным исходом в общей массе злокачественных заболеваний крови достаточно мала (1,5-2%), тенденция к старению всего населения Земли, делает такую разновидность болезней всё чаще встречающейся.
На фото — миелобласты в окружении нормальных клеток крови
Подтип, заслуживающий пристального внимания и медицинских исследований – М4-миеломоноцитарный. По статистике он составляет до 15% от всех ОМЛ. Большая часть заболевших составляют латиноамериканцы в возрастной категории около 30 лет.
Хронический тип
Основным отличием хронического миелоидного лейкоза от острого является место скопления мутировавших лимфоцитных бластных клеток.
Хронический миелобластный лейкоз (ХМЛ) – это злокачественная патология, для которой характерно нерегулируемое деление зрелых и юных нейтрофилов, эозинофилов и базофилов.
Быстро и бесконтрольно размножаясь в костном мозге, они скапливаются не в нём, а в крови. Именно этот факт способствует более благоприятному течению болезни и прогнозу продолжительности жизни.
Исторически, ХМЛ стал первым лейкозом у которого была установлена конкретная причина его зарождения. По месту работы её первооткрывателей, эту специфическую мутацию 8 и 22 хромосом назвали «филадельфийской».
Возрастная категория больных с хроническим типом миелоидного лейкоза более молодая, чем у ОМЛ – болезнь чаще всего диагностируют после 30-40 лет, а самое большое количество болеющих – 50-летние.
Признаки и симптомы
Как правило, оба типа миелоидных лейкозов дебютируют без симптомов и на первой стадии своего развития обнаруживаются случайно – при выполнении общего (клинического) анализа крови, обусловленного плановой диспансеризацией или другими причинами. Если при таком исследовании фиксируется повышенное содержания базофилов, эозинофилов, разного «возраста» гранулоцитов и созревших миелоидных клеток, то можно предположить, что есть вероятность миелоидного лейкоза.
При сравнении симптомов острого и хронического разных типов миелобластных лейкозов, можно найти как одинаковые признаки, так и характерные отличия. Для острого типа характерны следующие симптомы:
- повышенная и быстрая утомляемость;
- потеря аппетита и веса тела;
- бледность кожных покровов;
- лихорадочные состояния;
- снижение сопротивления инфекциям;
- кровоточивость и подкожные гематомы;
- селезёнка и печень не увеличены;
- боль в костях и суставах;
- увеличение лимфоузлов встречается редко;
- у 10% развивается кожный лейкоз;
- синдром Свита – красные бляшки и папулы на лице;
- синдром ДВС.
Хронический миелобластный лейкоз, в его второй (хронической) фазе, можно распознать по таким симптомам:
- чувство переполнения живота;
- общее недомогание;
- потливость;
- снижение веса тела;
- подагра;
- учащение случаев инфекционных болезней;
- изменение количества тромбоцитов;
- повышенная кровоточивость;
- увеличение объёма селезёнки и печени;
- сердечные боли и аритмия;
- длительное повышение температуры в пределах 37,1-37,5 °C.
Диагностика
Для уточнения диагноза по типу и дифференциации подтипа применяются следующие диагностические методы и лабораторные анализы:
- биохимиия крови с лейкоцитарной формулой и СОЭ;
- цитостатика и цитохимия лейкоцитов крови и состава костного мозга, в том числе с применением светового микроскопирования, поточной цитометрии и флуоресцентной гибридизации in situ.
В диагностике ОМЛ важно точно установить тип и подвид лейкоза, а также отбросить наличие предлейкозных состояний, поскольку все они лечатся по-разному.
Для хронического типа важно квалифицировано определить присутствие филадельфийской хромосомы. Зачастую, такая аномалия может маскироваться другими дефектами.
Лечение острого и хронического миелоидного лейкоза
Лечение острого миелобластного лейкоза состоит из двух этапов:
- Индукция – направлен на уничтожение изменённых клеток. Для всех подтипов ОМЛ (исключение МЗ) применяется индукционная химиотерапия «7+3» (цитрабин + антрациклиновый антибиотик в первые 3 дня).
- Консолидация – длительное поддерживающее лечение, основная цель которого состоит в закреплении достигнутой полной ремиссии, преодолении последствий химиотерапии и предотвращении рецидивов. В зависимости от подтипа ОМЛ и состояния больного это может быть дополнительные 3-5 курсов химиотерапии или трансплантация стволовых клеток (в случае предшествование миелодисплазии или первичном рецидиве).
Своевременно начатое лечение хронического миелобластного лейкоза позволяет остановить развитие болезни в его второй фазе и не дать наступить следующим – фазе акселерации и бластному кризу, которые могут перерасти в ОМЛ.
Первичная (таргетная) терапия ХМЛ состоит в применении ингибиторов тирозинкиназы. Второй и самый главный метод – трансплантация гемопоэтических стволовых клеток. Если больному не показана трансплантация, то применяют гидреа- и интерферон-альфа-с или без цитарабина.
Острый тип
Для острого миелобластного лейкоза общий долгосрочный прогноз выживаемости колеблется в пределах от 20 до 40 процентов, а для молодых пациентов, перенёсших трансплантацию – от 40 до 50%. Для детей (до 15 лет) прогноз лучше, чем у взрослых. Можно рассчитывать на 5-летнюю выживаемость в 70%.
Самый неблагоприятный прогноз для жизни – всего лишь 15% и частотой возникновения рецидивов около 80%, можно отнести к ОМЛ с мутациями в 3,5 и 7 хромосомах. Лучшими шансами обладают больные с подтипами М2, М3 и М4. У них 5-летняяя выживаемость равна 70%, а риск развития рецидива снижен до 30%.
Хронический тип
Для хронического миелоидного лейкоза прогноз гораздо выше:
- 5-летняя выживаемость при своевременно начатой терапии «7+3» – 90%;
- при пересадке костного мозга – более 15 лет.
Если же ХМЛ вовремя не диагностировали, то прогноз для продления жизни крайне неблагоприятен.
Источник:
Поделиться:
Добавить комментарий